英格尔认证检测
英格尔认证检测
- 首页
- 关于我们
-
服务介绍
-
聚烯烃类
-
矿石分析
-
金属材料及制品分析
-
金属加工油
-
工业清洗剂
-
水处理剂分析
-
纺织制造用剂
-
建筑助剂
-
食品添加剂分析
-
化妆品分析
-
消毒剂/抗(抑)菌制剂
-
工程塑料
-
橡胶助剂
-
节能环保助剂
-
玩具道具
-
木材及玻璃助剂
-
选矿助剂
-
油田助剂
-
表面活性剂
-
印刷化学品
-
电子化学品
-
食品/保健品食品
-
中药
-
除草剂
-
杀虫剂
-
PVC
-
兽药
-
肥料
-
细胞组织试剂
-
诊断试剂
-
前处理剂
-
后整理剂
-
染色助剂
-
印花助剂
-
皮革助剂
-
石材助剂
-
其它建筑材料
-
污水处理剂
-
工业循环水处理剂
-
塑料助剂/母粒
-
橡胶
-
水产药剂
-
工业用油脂
-
车船用油脂
-
燃料用油
-
新型油品添加剂
-
切削液
-
金属加工液
-
商用清洗剂
-
民用清洗剂
-
电镀药水/添加剂
-
化学镀添加剂
-
磷化液
-
钝化液
-
净化吸附类产品
-
烟草及电子烟
-
胶黏剂
-
油漆涂料
-
油墨
-
中药材
-
食品
-
饲料
-
阻垢剂
-
除垢剂
-
絮凝剂
-
反渗透药剂
-
精细助剂
-
产品毒性/安全性测试
-
测试
-
电子化学品行业
-
高纯电子级化学品
-
功能性电子化学品
-
成分分析
-
超纯水
-
食品热点测试项目
-
- 动态资讯
- 联系我们
- 首页
- 关于我们
-
服务介绍
- 医药
-
检测
第三方检测机构
眼镜检测 攀岩项目检测 小家电产品检测 净化材料检测 工业CT扫描检测 预埋滑槽性能检测 抗震支吊架、托臂支架、综合管廊支架性能检测 洁净室综合性能检测服务 半导体服务 英格尔汽车检测 土壤普查服务 消毒产品病毒灭火检测 防火阻燃检测服务 日化产品质检 净化产品 油品 绿色工厂 英格尔半导体服务 小家电检测页面 半导体洁净度检测 AMC监控检测 半导体洁净度检测 空气过滤器检测 锂电池检测 特气管道检测 新风机检测 特种设备检测 空气净化器检测 塑胶跑道检测 家具成品检测 涉水产品检测 油墨测试 油漆涂料测试 英格尔研发分析中心 胶水检测 电线产品检测 金属检测 塑料检测 橡胶测试 建材检测 消防安全 英格尔测试中心 智能家居检测 健身器材 智能装备检测 涉水 家具用品测试 分析测试 食品接触材料检测 老化试验 成分分析 硫化物测试 阻燃检测 测试方案咨询 电子化学品 安全性/毒理性测试 费用 工业诊断 环境检测 香精香料 配方分析 材料分析测试 元素分析 成分分析 塑胶跑道检测认证 产品研发 未知物检测分析 第三方检测 精细化学品
-
认证
管理体系认证
ISO56005创新管理-知识产权管理认证 ISO56002创新管理体系认证 ISO37001反贿赂管理体系认证 ISO31000风险管理体系认证 ISO55001资产管理体系认证 ISO37301合规管理体系认证 ISO22301业务连续性管理体系认证 ISO28000供应链安全管理体系 ISO27701隐私信息管理体系认证 ISO22000食品安全管理体系 GB/T31950企业诚信管理体系 GB/T 23794企业信用等级评价 综合认证服务 ISO45001 职业健康体系认证 售后服务认证 绿色产品认证 防疫用品检测 电器认证服务 HACCP体系认证 ISO20000 信息技术管理体系认证 GB/T50430工程建设施工管理体系认证 ISO27001信息安全体系认证 ISO50001能源管理体系认证 ISO13485医疗器械体系认证 ISO9001质量管理体系认证 ISO14001环境管理体系认证
-
分析
- 培训
- 智慧能源
- 动态资讯
- 联系我们

我们为药包材& 生产工艺系统相容性研究产业提供
一站式技术服务
药包材& 生产工艺系统相容性研究
- 药包材相容性研究简介

药包材与药物相容性试验是为考察药包材与药物之间是否会发生相互的或单方面的迁移,进而影响药品质量而进行的试验,其目的是通过相容性试验证实药品在整个使用有效期内,所选包装容器中的药品质量稳定、可控,能够保持其使用的安全性和有效性。
常用的药包材种类有塑料、玻璃、金属和橡胶。由于药包材的种类、组成和配方不同,其物理和化学的性能差异很大,在其包装药物后对各类药物的影响也就不同,所以,对不同的药包材,在进行与药物相容性试验时的考察项目、采用的方法和结果的评价等也均不相同。
- 业务范围
1、包材:
安瓿瓶、西林瓶、卤化丁基胶塞、预灌封、卡式瓶、塑料输液袋、药用塑料软膏管、气雾剂喷雾阀门、抗生素铝塑组合盖等。
2、一次性使用系统SUS:
硅胶软管、滤芯、一次性储液袋、不锈钢针头等
技术支持:CFDA、FDA、ICH、USP、BPDG等相关指导原则
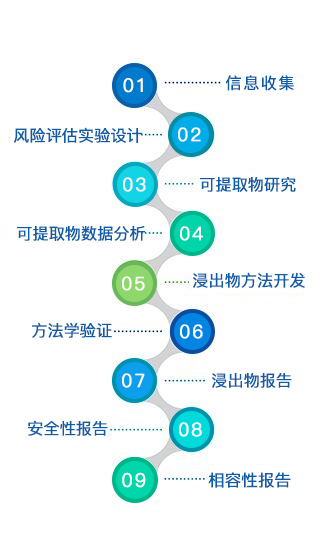
- 药包材相容性流程研究
1. 信息的收集评估
根据项目申请单的包装材料配方信息、生产工艺信息以及与药品有关的关键参数(如规格、给药途径、日最大摄入量等)为客户定制相容性研究方案。
2. 提取实验和模拟试验
模拟、提取试验会充分考虑药品在生产、贮存、运输以及使用过程中可能面临的极端条件进行阈值的计算、模拟液和模拟条件的选择、以及对可提取物方法的开发,帮助客户筛选包材。
3. 方法学设计与验证
根据中国药典及国内相关指导原则,对检测方法进行方法学验证,包括专属性、线性、精密度、回收率、检出限和定量限。
4. 浸出物(迁移)试验
针对加速、长期稳定性样品的测试,根据CFDA药品研发试验记录规定规范原始数据管理。
5. 毒理学安全性评估
参考毒理学数据库如DEREK, TOXNET, HSDB, TOXLINE等,由毒理学专家完成包括建模、数据库查询、文献查询、阈值计算等工作,从而得到完整的毒理学评估报告。
6. 结论
由提取和迁移试验,并参考毒理学评估结果,给予客户最后的相容性结论。
《化学药品注射剂与药用玻璃包装容器相容性研究技术指导原则(试行)》 《化学药品注射剂与塑料包装材料相容性研究技术指导原则(试行)》 《化学药品注射剂与药用弹性体相容性研究技术指导原则(试行)》 《YBB00142002-2015药品包装材料与药物相容性试验指导原则》 《中国药典》2015版等
包装材料和药品种类多样、复杂 法规要求理解不透彻,无法设计出一套完整的解决方案 溶出量极低且体系复杂,仪器的高灵敏度和高选择性并重
深入研究包材配方及药品的详细信息,明确需要考察的重点 结合国内政策及药学专家数年的研究经验来制定专属相容性研究方案 配置一整套新的、敏度高、带审计追踪功能的仪器设备(包括但不限于AB SCIEX LC-MS-MS、PerkinLmer ICP-MS/OES、安捷伦HPLC-FID/DAD、GC-MS-MS等) |
|